3.5.5. Лечение.
Лечение полиурической ОПН сводится к значительному увеличению объема вводимой жидкости (до 8-10 л в сутки), содержащей препараты калия. Для увеличения выделение веществ, которые реабсорбируются в почечных канальцах (мочевины, калия, натрия и других) возможно введение мочегонных препаратов. Креатинин не подвергается реабсорбции, поэтому на его уровень такой способ лечения не влияет. При снижении объема выводимой мочи допустимо применение эуфиллина, а также допамина в дозе 0,5-1,5 мкг/кг•мин, хотя ряд исследователей высказывает сомнения в эффективности применения этих средств (C.A. Block, H.L. Manning, 2002; J.A.Kellum, J.M. Decker, 2001).
Основная лечебная доктрина при олигурической ОПН состоит в обеспечении максимально возможного кровотока в почках с коррекцией гиперазотемии и водно-электролитных расстройств. Главная проблема – оптимальный волемический статус. Для профилактики ОПН и на начальных этапах ее развития необходима борьба с гиповолемией за счет адекватной инфузионной терапии. Возможно также использование симпатомиметиков для поддержания перфузии почек. Однако значительное несоответствие диуреза и объема вводимой жидкости при нарастании олигурии и развитии анурии вызывает гипергидратацию. Она приводит к отеку и дисфункции паренхиматозных органов – мозга, легких, печени, самих почек. В связи с этим наиболее сложным моментом в волемической тактике является ее своевременное радикальное изменение: переход от регидратации к дегидратации. Дегидратация возможна при использовании медикаментозных средств – салуретиков (фуросемид до 1000 мг/сут, по некоторым данным, лучше в режиме постоянной инфузии), а также симпатомиметиков. Более эффективной является аппаратная дегидратация. При разрешении анурии и развитии полиурии вновь возвращаются к регидратации.
При олигурической ОПН важен контроль над концентрацией электролитов в крови и коррекция следующих нарушений:
•гиперкалиемии (ограничение экзогенного калия и введение кальция);
•гипермагниемии и гиперфосфосфатемии (применение алюминий-содержащих антацидов, например фосфалюгеля, показано для связывания фосфатов, а магний-содержащих, например альмагеля, противопоказано);
•гипонатриемии (введение натрия).
Вне зависимости от формы истинной ОПН обязательна профилактика желудочно-кишечных кровотечений и сопровождающего их синдрома диссеминированного внутрисосудистого свертывания (ДВС). Желудочно-кишечные кровотечения возникают из-за выделения слизистыми оболочками уремических токсинов и их раздражающего действия. Кроме того, уремические токсины угнетают выработку VIII фактора свертывающей системы крови и тромбоцитов. Своевременное энтеральное питание, применение Н2-блокаторов (например, циметидина) и ингибиторов протонной помпы (омепразола), введение свежезамороженной плазмы являются средствами профилактики этих патологических состояний. При проведении искусственного питания акцент делается на углеводы и жиры, количество белков ограничивается из-за азотемии. В структуре консервативной терапии ОПН обязательно снижение дозировок лекарств, выводимых почками.
При неэффективности консервативных мероприятий используют экстракорпоральные методы (табл.6).
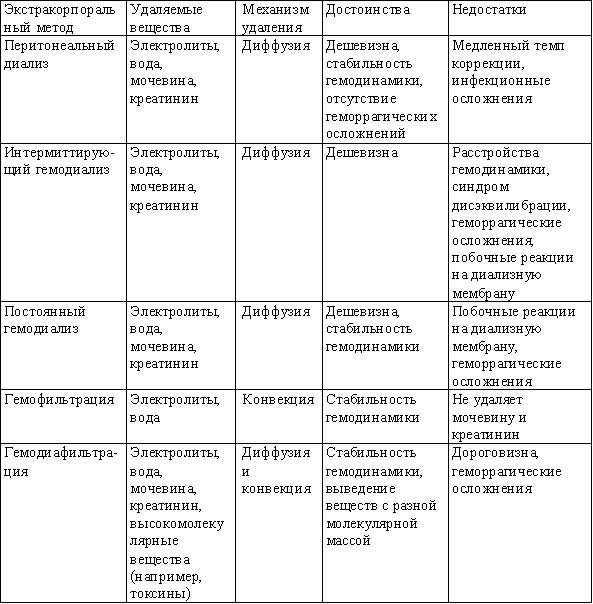 Табл.6. Достоинства и недостатки экстракорпоральных методов лечения почечной недостаточности
Табл.6. Достоинства и недостатки экстракорпоральных методов лечения почечной недостаточности
Экстракорпоральные методы раделяют на постоянные и интермиттирующие. Постоянные методы – гемофильтрация (ультрафильтрация), гемодиафильтрация и постоянный гемодиализ. В зависимости от места забора крови и возврата ее в организм постоянные методы могут быть артериовенозными или веновенозными. При использовании постоянных методов во внешнее устройство (диализатор, фильтр) выводят небольшие объемы крови, подвергающиеся очистке. Благодаря этому практически никогда не отмечается серьезных гемодинамических нарушений при использовании этих методов. Эффективность очищения крови достигается длительностью процедуры. В интермиттирующем режиме могут использоваться гемодиализ и перитонеальный диализ. Большие объемы выводимой жидкости, особенно при интермиттирующем гемодиализе, создают опасность гемодинамических расстройств, поэтому в настоящее время этот метод практически не используют при неотложных состояниях.
Гемофильтрация (ультрафильтрация) является методом быстрого удаления жидкости и солей посредством пропускания потока крови через волоконные фильтры. Механизм удаления – конвекция. Преимуществом является быстрота коррекции водно-электролитных нарушений при сохранении гемодинамической стабильности. В качестве серьезного недостатка следует отметить тот факт, что при гемофильтрации практически не удаляются азотистые соединения.
При гемодиализе происходит быстрое удаление жидкости, солей и азотистых соединений посредством выведения части внутрисосудистого объема крови в диализатор с полупроницаемыми мембранами. В диализаторе создается противоточный механизм за счет встречных потоков крови и диализата. Механизм удаления – диффузия. Преимуществом гемодиализа является быстрота коррекции водно-электролитных и азотистых расстройств, а также дешевизна метода. Существуют два основных недостатка метода: гемодинамическая нестабильность из-за «экстравазации» крови (ее выведения из сосудистого русла в диализатор) и дисэквилибрические нарушения. Постоянный гемодиализ проводят с низкими скоростями крови и диализата, поэтому указанные недостатки значительно нивелированы. Возможны побочные реакции на диализную мембрану, которые зависят от ее типа, а также геморрагические осложнения из-за использования гепарина с целью предупреждения тромбирования магистралей диализатора.
Гемодиафильтрация представляет собой метод, сочетающий принципы гемофильтрации и гемодиализа. Гемодиафильтрация – это гемофильтрация с одновременным созданием противотока диализата. Механизмы удаления – конвекция и диффузия. Гемодиафильтрация сочетает преимущества гемофильтрации и гемодиализа: гемодинамическая стабильность при хорошем удалении воды, электролитов и азотистых соединений. Недостатком метода является высокая стоимость процедуры из-за необходимости возмещения больших объемов удаляемой воды и электролитов (калия, магния, натрия, кальция) – до 30-35 л/сут.
При перитонеальном диализе происходит медленное удаление жидкости, солей и азотистых соединений посредством создания осмотического градиента между кровью и введенным в брюшную полость гипертоническим раствором. Механизм удаления – диффузия через брюшину. Преимуществом перитонеального диализа является удаление азотистых соединений при отсутствии гемодинамической нестабильности. Проведение перитонеального диализа не сопровождается увеличением риска геморрагических осложнений, неизбежно присущих любому аппаратному методу, при котором используется гепарин с целью поддержания текучести крови через внешнее устройство. Недостатки метода – медленный темп коррекции и возможные инфекционные осложнения из-за нарушения замкнутости брюшной полости.
При использовании экстракорпоральных методов необходимо обращать внимание на некоторые принципиальные моменты. Первый момент – это стабильность центральной гемодинамики. Если при проведении экстракорпоральной очистки крови отмечаются эпизоды артериальной гипотонии, то это сказывается на церебральном и почечном кровотоке из-за нарушений их ауторегуляции и задерживает восстановление функции мозга и почек. Для профилактики расстройств гемодинамики в диализатор не следует выводить одномоментно большие объемы крови, потери жидкости предпочтительно возмещать гиперосмолярными растворами натрия. Кроме того, необходимо уменьшение температуры диализата.
Второй важный момент – предупреждение дисэквилибрических расстройств. Нельзя быстро выводить мочевину и креатинин из крови. При медленном выведении азотистых соединений посредством экстракорпоральных методов в кровь по градиенту концентрации постепенно поступают мочевина и креатинин, накопившиеся в легких, мозге и других внутренних органах. Поступление их в кровь сопровождается постепенным удалением из организма. Градиент концентрации мочевины и креатинина между тканями и кровью одновременно является градиентом концентрации воды. В связи с этим вместе с мочевиной и креатинином, поступающими из тканей в кровь, идет и обратный процесс – поступление воды из крови в эти ткани. Медленный темп выведения азотистых соединений из организма не создает опасности перемещения больших объемов воды из внутрисосудистого сектора в интерстициальный и внутриклеточный. При быстром темпе выведения азотистых соединений они не успевают выйти из тканей и остаются в них в большой концентрации. Туда по осмотическому градиенту начинает поступать вода из крови. Из-за относительной гиповолемии возникают расстройства гемодинамики. Из-за гипергидратации тканей развиваются отек легких и мозга. Последний особенно опасен у пациентов с ЧМТ из-за имеющейся у них исходной внутричерепной гипертензии. Дисэквилибрические расстройства из-за поспешного снижения азотистых соединения в крови – основная причина гибели пациентов с ЧМТ после применения экстракорпоральных методов.
Третий важный момент – это использование гепарина для поддержания текучести крови в магистралях аппарата. Из-за опасности рецидива внутричерепного кровоизлияния доза этого препарата должна быть минимальной.
В заключение раздела приведем практический алгоритм оценки нарушений темпа диуреза при черепно-мозговой травме. Традиционно диурез, наряду с уровнем АД и характером дыхания, является одним из наиболее привлекающих внимание реаниматологов показателей.






